- 1. L’évaluation préthérapeutique des hémopathies
- 2. Les anémies
- 3. Les leucémies aiguës
- 4. La leucémie lymphoïde chronique
- 5. Les lymphomes malins non hodgkiniens
- 6. Le lymphome hodgkinien
- 7. Les syndromes myélodysplasiques
- 8. Les syndromes myéloprolifératifs [1]
- 9. La leucémie myéloïde chronique
- 10. Le myélome multiple
7. L’allogreffe de cellules souches hématopoïétiques
L’allogreffe est une immunothérapie qui consiste à transférer des cellules souches hématopoïétiques à un patient qui a reçu des doses intensives de chimiothérapie ou de radiothérapie (conditionnement).
L’action antitumorale résulte de l’action du conditionnement ainsi que de l’effet « greffon versus leucémie » (graft versus leukemia [GVL]).
L’indication d’allogreffe se pose dans des pathologies résistantes aux stratégies thérapeutiques conventionnelles ou à haut risque de rechute et dépend de plusieurs critères liés au patient tels que [11] :
- état général, performance status (PS) ;
- comorbidités ;
- pathologie d’origine.
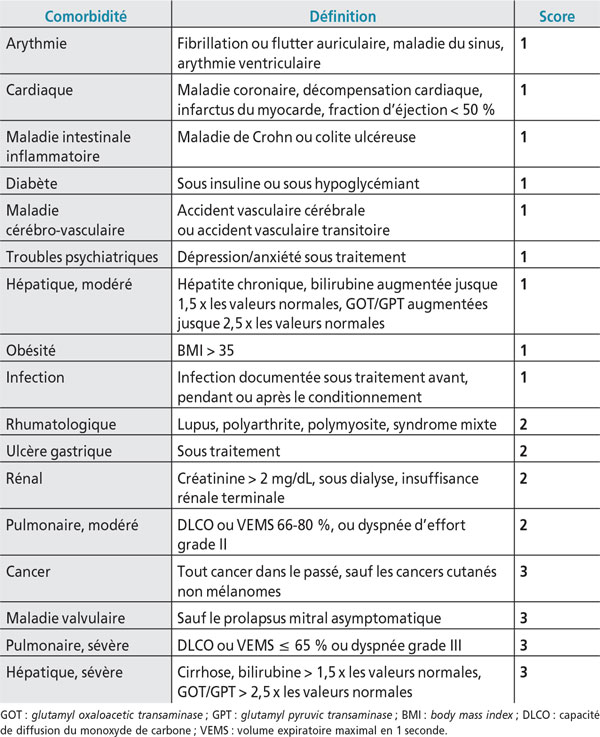
Le score de Sorror [Tableau I] permet d’évaluer l’éligibilité du patient à cette stratégie thérapeutique en fonction des comorbidités [12]. Plus le score est élevé, moins les chances de réussite de la greffele sont.
[Tableau I] Hematopoietic cell transplant-comorbidity index (HCT-CI ou score de Sorror) (d’après [13]).
La recherche de donneur commence par la fratrie si cela est possible,
elle se poursuit par la recherche d’un donneur compatible sur le registre national et les registres internationaux.
Typage HLA
La sélection des donneurs dépend du typage HLA (antigènes des leucocytes humains). La recherche porte sur différents anti- gènes : A, B, C, DR et DQ. La recherche est plus restreinte pour le sang de cordon (antigènes A, B, DR). Une compatibilité sur latotalité des antigènes correspond à un donneur HLA 10/10 (identique pour les deux allèles HLA). Une incompatibilité sur un antigène (mismatch) correspond à un donneur HLA 9/10.
Type de donneurs
• Géno-identique : donneur intrafamilial (fratrie HLA 10/10)
• Phéno-identique : donneur sur fichier (HLA 10/10 ou 9/10)
• Unité de sang placentaire : sang de cordon (HLA 6/6, 5/6 ou 4/6)
• Haplo-identique : donneur familial (HLA 5/10)
Type de dons
• Moelle osseuse : prélèvement au bloc opératoire de la moelle osseuse du donneur par biopsie
• Cellules souches périphériques : récupération des cellules souches par cytaphérèse après stimulation par facteurs de croissance
• Sang placentaire : sang riche en cellules souches hématopoïétiques recueilli après la délivrance par cathétérisme du cordon ombilical et collecte du contenu sanguin placentaire
Conditionnements
Une fois que le donneur a été trouvé, il faut déterminer le type de conditionnement qui va être administré avant l’allogreffe :
- conditionnement standard myélo-ablatif ;
- conditionnement myélo-ablatif d’intensité réduite ;
- conditionnement non myélo-ablatif ;
- conditionnement séquentiel.
L’objectif du conditionnement est de détruire les cellules souches de la moelle osseuse et d’abaisser les défenses immunitaires du patient afin de diminuer le risque de rejet du greffon. En revanche, il existe un risque de réaction du greffon contre l’hôte (GVH : graft versus host). Ce risque dépend de nombreux facteurs : âges du patient et du donneur, type de conditionnement, type de greffon, incompatibilité HLA, etc. La difficulté est de trouver un équilibre entre l’effet GVH et l’effet GVL [11].
Immunomodulation post-greffe
Les immunosuppresseurs
Les immunosuppresseurs sont les traitements utilisés pour lutter contre la GVH. Le suivi post-allogreffe des patients permet de trouver l’équilibre entre la GVH et la GVL. Les traitements immunosuppresseurs sont ajustés en fonction du pronostic initial de la maladie, du statut de la maladie et du risque de rechute.L’état général du patient en fonction du PS, des réactivations virologiques, du grade de GVH, permet d’ajuster au mieux les traitements dont l’objectif est d’obtenir une guérison sans rechute avec une qualité de vie maximale. Contrairement aux greffes d’organes solides, les immunosuppresseurs seront arrêtés progressivement avec l’installation d’une tolérance entre le greffon et l’hôte [14].
Injection de lymphocytes du donneur
Les lymphocytes du donneur ou Donor Lymphocytes Infusion (DLI) permettent de renforcer l’activité de la greffe par réinjection intraveineuse de lymphocytes issus du donneur de cellules souches hématopoïétiques. Les lymphocytes sont réinjectés à dose croissante en fonction de la compatibilité et de l’indication, et doivent être stoppés chez les patientsdéveloppant une GVH à un grade > ou égal à 2.
Les DLI sont indiquées en cas de rechute en association avec des traitements (chimiothérapie, thérapie ciblée). Ils sont également utilisés en prophylaxie chez les patients pour lesquels le diagnostic initial présentait un caryotype complexe avec un pronostic défavorable et un taux de rechute important. Dans ce cas, les DLI sont associés à une baisse précoce et rapide des immunosuppresseurs dans les 100 jours après l’allogreffe et les réinjections débutent 1 mois après l’arrêt total de ceux-ci. Enfin, certains paramètres tels que le chimérisme mixte (apparition de cellules du receveur sur les lymphocytes T CD3+ supérieur à 5 %) ou le suivi de la maladie résiduelle peuvent inciter à programmer des DLI préemptifs [15].
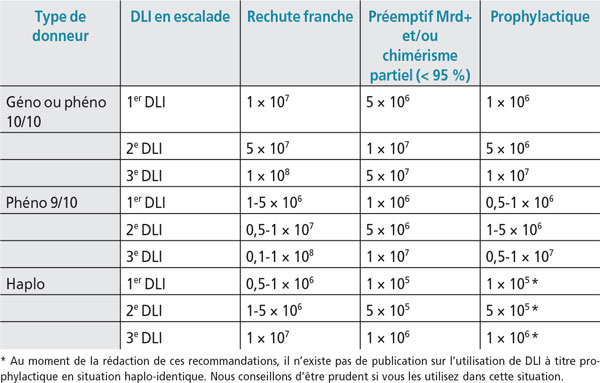
[Tableau II] Doses de DLI préconisées (CD3/kg du receveur) [15].
Cette réinjection peut se faire sur voie veineuse centrale ou périphérique en hôpital de jour. Une prémédication peut être envisagée (antihistaminique et hydratation avec une solution saline), une surveillance rapprochée avec prise de constantes (pouls, tension artérielle, température et saturation) est nécessaire durant la réinjection et les 2 heures qui suivent celle-ci.
Risques liés à la greffe
Infectieux : Le statut immunitaire des patients entraîne un risque important d’infections (virales, parasitaires, bactériennes, fongiques). Après la greffe de cellules souches, les patients prennent pendant plusieurs mois des traitements à visée prophylactique et/ou curative en fonction de leurs analyses sanguines, leurs constantes vitales,leurs symptômes.
GVH : Le risque de GVH étant majeur, la GVH (réaction du greffon contre l’hôte) est recherchée car associée à un effet GVL (réaction du greffon envers les cellules malignes) mais doit être contrôlée car elle peut entraîner de lourdes complications cutanées, digestives, hépatiques [16].
Réaction du greffon contre l’hôte
C’est la réaction immunitaire des cellules du donneur contre les tissus du receveur.
Il existe deux types de GVH :
La GVH aiguë
Elle survient dans les 100 jours après la greffe et peut atteindre différents organestels que la peau, les intestins et le foie [11].
La GVH chronique
Elle survient de 100 jours à plus d’un an après la greffe et peut atteindre différents organes tels que la peau, les yeux, le système digestif, le foie et les poumons.
La stratégie thérapeutique de ces affections réside dans l’utilisation de thérapeutiques immunosuppressives [11].
Rechute : la rechute est possible, les traitements dépendront du type de maladie et du délai entre la greffe et la rechute.Plus la rechute survient tôt après la greffe, plus elle est difficile à traiter.
Rejet : complication plus exceptionnelle, le patient ne sort pas d’aplasie, une deuxième greffe peut alors être envisagée.
Les autres risques liés aux traitements immunosuppresseurs, aux chimiothérapies, à la radiothérapie : cataracte, ostéoporose.

